Аммиак – это летучее водородное соединение (нитрид водорода), которое играет ведущую роль в современной промышленности.
Хоть его и открыли лишь в восемнадцатом веке, но он был известен человеку с незапамятных времен. Водный раствор аммиака – это нашатырный спирт. Данное вещество содержится в продуктах разложения живых организмов и моче. Поэтому при распаде органики (останков растений, животных) выделяется аммиак, и от этого появляется резкий запах гниения (нашатыря).
История аммиака
Аммиак был открыт в конце восемнадцатого века британским химиком Джозефом Пристли – одним из основоположников современной химии, который совершил также множество важных открытий в других сферах науки (физике, биологии, оптике).
Например, в списках его изобретений есть: газированная вода, за которую он получил медаль Лондонского Королевского общества, и всем известный ластик (раньше для стирания графита все пользовались хлебом).
Нельзя отрицать того, что Джозеф Пристли сделал огромный вклад в химию, особенно в области газов, однако многие свои достижения он совершил случайно.
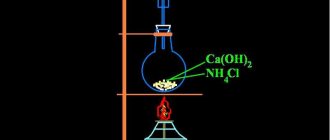
Джозеф Пристли получил аммиак методом нагревания хлорида аммония (нашатырь) с гидроксидом кальция (гашеная известь) и затем собрал выделившийся газ в ртутной ванной.
Ртутная ванная – это специальный прибор, созданный Пристли для концентрирования газов. При комнатной температуре ртуть является жидкостью с высокой плотностью, что не позволяет ей абсорбировать газы. Их ученый легко выделял из веществ, нагревая над поверхностью ртути.
Уравнение аммиака:
2NH4Cl + Ca(OH)2 = NH3 + CaCl2.
После открытия Джозефом Пристли аммиака, его изучение не стояло на месте.
В 1784 был установлен состав этого вещества химиком Луи Бертолле, который разложил его на исходные элементы электрическим разрядом.
Именование «нашатырь» он получил уже в 1787 году от латинского названия нашатырной щелочи, а само наименование «аммиак», которым мы привыкли пользоваться, ввел Яков Дмитриевич Захаров в 1801 году.
Но вот что интересно. За сто лет до Джозефа Пристли и его открытия аммиака, ученый Роберт Бойль наблюдал некое явление, при котором палочка, предварительно смоченная в соляной кислоте, начинала дымить, когда ее подносили к газу, выделяющемуся при сжигании навоза. Это объясняется тем, что кислота и аммиак вступали в реакцию, и в ее продуктах содержался хлорид аммония, частицы которого и создавали дым. Получается, что экспериментальными методами аммиак был выявлен давно, но его нахождение в мире было доказано намного позже.
Применение нашатырного спирта в быту
Аммиачная вода используется в садоводстве, а также в быту, как универсальное чистящее средство. Ее используют в борьбе с тлей, для обработки культурных посадок на участке от луковой мухи и для подкормки растений. Используют аммиак (нашатырный спирт) следующим образом:
Рецепт №1 — от тли:
- 4 ст. л. препарата разводят в 20 л воды. Количество можно менять, исходя из такой концентрации под нужный объем.
- Добавьте в раствор немного стирального порошка (для лучшего прилипания).
- Используйте раствор для опрыскивания растений при борьбе с тлей.
Рецепт №2 — удобрение
50 мл препарата растворите в 4 л воды. Используйте раствор как подкормку для огородных и комнатных растений.
Важно! Это средство также позволит избавиться от комаров и мошек.
Рецепт №3 — для полива лука
- Разводите 1-2 ст. л. нашатыря в ведре воды.
- Поливаете лук полученным средством — с момента посадки и до конца июня.
Рецепт №4 — чистка золота
- Смешайте 2 ч. л. нашатыря с 2 стаканами воды.
- Добавьте в раствор 1 ст. л. любого моющего средства.
- Поместите в чистящий раствор золотые украшения на 1-2 часа.
- После обработки, изделия промойте в воде и насухо протрите салфеткой.
Важно! Для чистки золота, это средство можно использовать и другим способом:
- Добавьте 0,5 ч. л. нашатырного спирта в 100 мл воды.
- В раствор добавьте 30 мл перекиси водорода и ½ ч. л. жидкого моющего средства.
- Поместите украшение в приготовленный раствор на 15 минут.
- После обработки золото промойте водой и насухо протрите салфеткой.
Способы получения
В мире ежегодно производится около 100 миллионов тонн аммиака, поэтому этот процесс можно по праву считать одним из важнейших в мире. Выпускают его в жидком виде или как двадцати пяти процентный раствор.
Существуют следующие способы его получения:
1. В промышленности аммиак добывают посредством синтеза азота и водорода, что сопровождается выделением тепла. Причем данная реакция может проходить лишь при высокой температуре, давлении и в присутствии катализатора, который, ускоряя слабую реакцию, сам в нее не вступает.
Уравнение реакции аммиака:
N2 + 3H2 ⇄ 2NH3 + Q
2. Можно получить аммиак во время коксования каменного угля.
На самом деле в угле нет никакого аммиака, но в нем присутствует много органических соединений, в составе которых содержатся азот и водород. А при сильном нагревании угля (пиролизе) эти составляющие и образуют аммиак, который выходит как побочный продукт.
3. В лаборатории аммиак добывают нагреванием хлорида аммония и гидроксида кальция:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3↑ + 2H2O
4. Или нагреванием хлорида аммония с концентрированной щелочью:
NH4Cl + NaOH = NaCl + NH3↑ + H2O
Что это такое?
Основное название — гидроксид аммония, в международном варианте — Ammonium Hydroxide. Это слабое соединение, полученное посредством смешивания аммиака с молекулами воды. Упоминается в ГОСТ Р 53045-2008, п.87.
Синонимичные названия:
- Е 527 (Е–527), европейский код;
- гидрат аммиака;
- гидрат окиси аммония;
- аммиачная вода;
- аммиак водный;
- едкий аммиак;
- едкий аммоний;
- нашатырный спирт;
- во Франции — hydroxid de ammonium;
- в Германии — Ammoniumhydroxid.
Виды
- Для пищевой, медицинской и косметической отраслей.
- Для сельскохозяйственной отрасли.
Описание и свойства
| Показатель | Стандарт |
| Внешний вид | Прозрачная бесцветная жидкость (иногда желтый оттенок). |
| Состав |
|
| Запах | Резкий характерный. |
| Растворимость | Высокая. |
| Содержание основного вещества | Не меньше 27%. |
| Вкус | Специфический. |
| Плотность | 0,91 (раствор 25%) г/см³. |
| Другое |
|
К какому классу относится?
Гидроксид аммония относится к регулятором кислотности и является сырьем синтетического происхождения.
Из чего и как получают?
Добавку Е527 получают путем соединения очищенной воды и аммиака. Для этого используются продукты сжигания каменного угля, после чего их растворяют в воде.
Процесс производства проходит в несколько этапов:
- дистилляция;
- дефлегмация;
- конденсация аммиачной воды.
Добавку Е527 производят российские предприятия:
- ОАО «Акрон» (город Великий Новгород);
- химическая (Тульская область);
- ОАО «Тольяттиазот».
Ведущие зарубежные производители:
- Knuchel Farben AG (Германия);
- Cutrin (Финляндия);
- Lubon Industry Co., Ltd.(Китай).
Применение
Аммиак – это незаменимое и действительно нужное вещество, без которого мировая промышленность замедлила бы свое движение. Область его применения широка: он задействован во всех производственных процессах человека, начиная от заводов и лабораторий, заканчивая медициной. Его преимущества в том, что он экологически чист и является довольно дешевым продуктом.
Области применения аммиака:
- Химическая промышленность. Его используют в производстве удобрений, полимеров, азотной кислоты, взрывчатых веществ, в качестве растворителя (жидкий аммиак).
- Холодильные установки. Аммиак испаряется с поглощением большого количества тепла из окружающей среды, так как обладает определенными термодинамическими свойствами. Холодильные системы, основанные на его применении более чем эффективны, поэтому он является главным хладагентом в промышленности.
- Медицина. Нашатырный спирт или 10 % раствор аммиака используют при выведении из обморочного состояния (раздражение рецепторов слизистой оболочки носа способствует стимуляции дыхания), обработке рук хирурга, возбуждении рвоты и так далее.
- Текстильная промышленность. С его помощью получают синтетические волокна. Также аммиак используют при очистке или окрашивании различных тканей.
Как узнать, что гидроксид аммония есть в составе товара?
Всю информацию о наличии данной добавки производитель отражает на этикетке продукта, в конце списка, вместе с остальными регуляторами кислотности, эмульгаторами и консерваторами. Чаще всего ставится отметка Е527, а в скобках указывается расшифровка — гидроксид аммония.
Иногда Е527 можно встретить под названием гидрат аммиака или гидрат окиси аммония. На иностранной продукции используется международное название Ammonium Hydroxide или европейский код Е-527. В медицинских препаратах добавка отмечается как нашатырный спирт.
Физические свойства
Вот какие физические свойства присущи аммиаку:
- При нормальных условиях является газом.
- Бесцветный.
- Имеет резкий запах.
- Ядовит и очень токсичен.
- Очень хорошо растворим в воде (один объем воды на семьсот объемов аммиака) и ряде органических веществ.
- Температура плавления составляет -80 °С.
- Температура кипения – около -36 °С.
- Является взрывоопасным и горючим веществом.
- Примерно вдвое легче воздуха.
- Имеет молекулярную кристаллическую решетку, соответственно, он легкоплавкий и непрочный.
- Молярная масса аммиака равна 17 грамм/моль.
- При нагревании в кислородной среде разлагается на воду и азот.
Как вывести пятна аптечным препаратом
Эффективное средство для удаления пятен — это нашатырный спирт. Там, где не справились современные моющие химикаты, раствор аммиака показывает отличные результаты. Нашатырный спирт нашел применение в чистке ковров, мягкой мебели, верхней одежды. После нанесения на поверхности неприятный запах раствора быстро улетучивается, а от жира и масла не остается и следа. Для выведения пятен с замшевой обуви или сумки следует нанести раствор на ватный диск и смочить область загрязнения. При необходимости процедуру можно повторить несколько раз до полного очищения поверхности.
Совет
Нельзя использовать для очищения 10%-й аптечный препарат, так как он чрезмерно агрессивно воздействует на ткани. Оптимальная концентрация раствора для выведения пятен — 2%. Чтобы его приготовить, следует к одной части 10%-го нашатырного спирта добавить пять частей воды и тщательно взболтать.
Нужно правильно развести аммиак, и нашатырный спирт очистит поверхности в течение нескольких минут. В отличие от бытовой химии, он не образует пену, от которой хозяйкам бывает трудно избавиться. Чтобы пятно исчезло после первой обработки, необходимо нанести на него свежеприготовленный раствор и легко втереть в тканевую поверхность. Закрепить результат можно, постирав одежду в стиральной машинке в обычном режиме.
Химические свойства аммиака
Аммиак является сильным восстановителем, так как степень окисления азота в молекуле минимальная. Он способен также к окислительным свойствам, что случается намного реже.
Реакции с аммиаком:
- С кислотами аммиак образует соли аммония, разлагающиеся при нагревании. С соляной кислотой аммиак составляет хлорид аммония, а с серной — сульфат аммония.
NH3 + HCL = NH4CL
NH3 + H2SO4 = (NH4)2SO4
- С кислородом при нагревании образуется азот, а при участии катализатора (Pt) получается оксид азота.
4NH3 + 5O2 = 4NO + 6H2O
4NH3 + 3O2 = 2N2 + 6H2O
- С водой образуется неустойчивый гидрат аммиака.
NH3 + H2O = NH3 × H2O
Аммиак способен проявлять щелочные свойства, поэтому при взаимодействии с водой он образует слабое основание – NH4OH. Но на самом деле такого соединения не существует, поэтому формулу следует записывать так: NH3 × H2O.
- С оксидами металлов.
2NH3 + 3CuO = 3Cu + N2 + 3H2O
- С галогенами.
8NH3 + 3Cl2 =N2 + 6NH4Cl
- С солями металлов.
3NH3 + ЗН2О + AlCl3 = Al(OH)3↓ + 3NH4Cl
Соединения аммиака
Есть несколько типов сложных веществ, образующихся при взаимодействии с аммиаком:
- Соли аммония. Они образуются в результате реакций аммиака с кислотами и разлагаются при нагревании.
- Амиды. Это соли, которые получают, действуя на щелочные металлы аммиаком.
- Гидразин. Это вещество, которое получают в результате окисления аммиака гипохлоритом натрия в присутствии желатина.
- Амины. Аммиак взаимодействует с галогеноалканами в качестве реакции присоединения, образуя соли.
- Аммиакаты. С серебром и солями меди аммиак образует комплексные соли.
Биологическая роль
Аммиак — вещество, образующееся в организмах живых существ при метаболизме, являющееся в них продуктом азотистого обмена. В физиологии животных для него отведена важная роль, однако он имеет высокую токсичность для организмов и почти не содержится в них в чистом виде. Большая его часть перерабатывается печенью в безвредное вещество – мочевину или как ее еще называют карбамид.
Также он способствует нейтрализации кислот поступающих в организм с пищей, поддерживая кислотно-щелочной баланс крови.
Аммиак – это важный источник азота для растений. Главным образом они поглощают его из почвы, но это очень трудоемкий и неэффективный процесс. Некоторые растения способны накапливать азот, который содержится в атмосфере, с помощью специальных ферментов – нитрогеназов. После чего они перерабатывают азот в полезные им соединения, например, белки и аминокислоты.
Агрегатные состояния
Аммиак может находиться в разных агрегатных состояниях:
- Он присутствует в виде бесцветного газа с неприятным резким запахом в нормальных условиях.
- Также он очень хорошо может растворяться в воде, поэтому его можно хранить в виде водного раствора с определенной концентрацией. Он сжижается и становится жидкостью в результате давления и сильного охлаждения.
- Аммиак имеет твердое состояние, в котором он предстает бесцветными кубическими кристаллами.
Итоговая таблица
А для удобства понимания, чем отличаются рассмотренные материалы, предлагаем итоговую таблицу:
| Вещество | Состояние | Химическое соединение | Формула | Применение | Свойства |
| Аммиак | Газ | Нитрид водорода | NH3 | Промышленность, удобрения | Без цвета. Резкий запах. |
| Нашатырный спирт | Жидкое | Гидроксид аммония | NH4OH | Медицина, удобрения | Без цвета. Резкий запах. |
| Нашатырь | Твердое | Хлорид аммония | NH4Cl | Удобрения, пищевая добавка, флюс | Порошок без запаха, белый |
Отравление аммиаком
Как уже выше упоминалось, аммиак – это крайне токсичное и ядовитое вещество. Его относят к четвертому классу опасности.
Отравление этим газом сопровождается нарушением многих процессов организма:
- Сначала поражается нервная система и снижается усвоение кислорода нервными клетками.
- При проникновении в глотку, затем трахею и бронхи аммиак оседает на слизистых покровах, растворяется, образуя щелочь, которая начинает пагубно действовать на организм, вызывая внутренние ожоги, разрушая ткани и клетки.
- Это вещество также оказывает разрушающее воздействие на жировые компоненты, которые в том или ином виде входят в состав всех органов человека.
- Попадают под влияние сердечно-сосудистая и эндокринная система, нарушается их работа.
После контакта с аммиаком страдает почти весь организм человека, его внутренние ткани и органы, ухудшается процесс жизнедеятельности.
Чаще всего случаи отравления этим газом происходят на химических производствах в результате его утечки, но также можно им отравиться и в домашних условиях, например, если емкость, в которой содержится нашатырный спирт, неплотно закрыта, и его пары накапливаются в помещении.
Отравление может произойти, даже когда при обморочном состоянии человеку подносят к носу тампон, смоченный в нашатыре. Если пострадавшему дать понюхать его более пяти секунд, то высок риск интоксикации, так что с нашатырным спиртом всегда следует обращаться предельно осторожно.
Симптомы отравления
Ниже перечислен ряд признаков отравления аммиаком:
- Сильный кашель, затруднение дыхания.
- Жжение в глазах, слезоточивость, болевая реакция на яркий свет.
- Жжение в полости рта и носоглотке.
- Головокружение, головная боль.
- Боли в животе, рвота.
- Снижение слухового порога.
- При более серьезном отравлении возможны: потеря сознания, судороги, остановка дыхания, острая сердечная недостаточность. Совокупность нарушений может привести пострадавшего в коматозное состояние.
Профилактика при отравлении
Первая помощь в данном случае состоит из нескольких простых действий. Сначала необходимо вынести пострадавшего на свежий воздух, промыть ему лицо и глаза проточной водой. Даже те, кто был не очень хорош в химии, со школы знают: щелочь нейтрализуется кислотой, поэтому ротовую полость и нос нужно обязательно промыть водой с добавлением лимонного сока или уксуса.
Если отравившийся потерял сознание, следует уложить его на бок на случай рвоты, а при остановке пульса и дыхания сделать массаж сердца и искусственное дыхание.
Влияние на организм: опасно ли вещество или нет?
Есть ли польза?
Установленной пользы для человеческого организма у добавки гидроксид аммония не выявлено.
Возможный вред и меры предосторожности
Важно! При длительном вдыхании аммиачных паров человек может получить ожог дыхательных путей, поэтому с растворами следует обращаться осторожно, хранить в плотно закрытых тарах, при работе с ними необходимо надевать специальную маску и защищать глаза очками.
Аммиак — активный раздражитель, способный негативно влиять на слизистые пищеварительного тракта, нарушить функциональность работы печени и почек. Поэтому нельзя нарушать максимально допустимую дозировку, а при первых признаках недомогания следует сразу обратиться за медицинской помощью.
Не стоит забывать, что пары аммония в больших концентрациях являются легковоспламеняющимися и взрывоопасными. Пожары, возникшие из-за аммиака, эффективней всего тушить пеной из огнетушителя.
Допустимое суточное потребление
Е527 добавляется в продукцию по техническим инструкциям производства, часто в комбинациях с иными гидроксидными добавками. Для пищевой промышленности в какао и шоколаде норма Е527 не должна быть больше 70 граммов на 1 кг. В других отраслях показатель снижен до 50 г на 1 кг.
Последствия отравления
После интоксикации аммиаком человека могут ждать очень серьезные необратимые последствия. В первую очередь страдает центральная нервная система, что влечет за собой целый ряд осложнений:
- Мозг перестает полностью выполнять свои функции и начинает давать сбои, из-за этого снижается интеллект, появляются психические заболевания, амнезия, нервные тики.
- Понижается чувствительность некоторых частей тела.
- Нарушается работа вестибулярного аппарата. Из-за этого человек ощущает постоянное головокружение.
- Органы слуха начинают терять свою работоспособность, что приводит к глухоте.
- При поражении глазных покровов снижается зрение и его острота, в худшем случае пострадавшего ждет слепота.
- Наступление летального исхода. Это зависит от того, насколько концентрация газа в воздухе была высокой и сколько паров аммиака попало в организм.
Знать и соблюдать предписанные меры безопасности — значит оградить себя от риска угрозы собственной жизни или худшей участи — инвалидности, потери слуха или зрения.